Mehrere, meist bösartige, Erkrankungen des Bluts oder Immunsystems können durch herkömmliche Therapien, inklusive hochdosierter Chemotherapie, nicht geheilt werden. Hier bietet die allogene Stammzelltransplantation, also die Transplantation von Stammzellen die durch eine:n verwandte:n Familien- oder unverwandte:n Fremdspender:in gespendet wurden, eine potentielle Heilungschance.
Die Behandlung mit Stammzellen
Bei der allogenen Stammzelltransplantation erhalten Patient:innen zuerst als Vorbereitung eine Konditionierungstherapie (hochdosierte Chemotherapie, oftmals Immuntherapie und selten auch Ganzkörperbestrahlung) und anschließend die gesunden Blutstammzellen des:der Spender:in, welche für die Blutbildung verantwortlich sind.
Neben Stammzellen befinden sich im Transplantat auch reife, langlebige Immunzellen, die die Aufgabe haben, fremde Zellen zu erkennen und zu attackieren. Hierdurch trägt das Spender:innen-Immunsystem dazu bei, residuelle Tumorzellen in dem:der Empfänger:in zu attackieren, und auch im weiteren Verlauf unter Kontrolle zu halten (sogenannter „Graft-versus-Leukemia“-Effekt). Bei der allogenen Stammzelltransplantation handelt es sich daher um eine Art „Immunzelltherapie“. Attackieren Spender:innen-Immunzellen hingegen gesunde Zellen und Gewebe des:der Patient:in, so spricht man von einer „Transplantat-gegen-Wirt-Reaktion“ (Graft-versus-Host-Erkrankung).
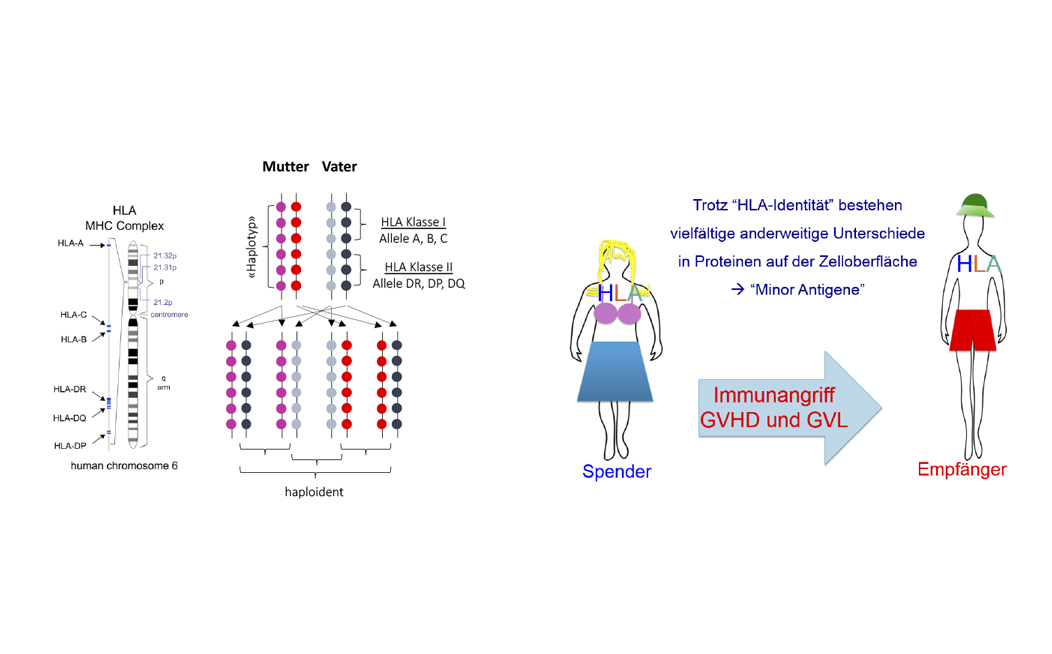
Damit diese Immunattacke des Spender:innen-Immunsystems sich nicht zu heftig gegen Zellen in dem:der Empfänger:in richtet, müssen sich Spender:in und Empfänger:in in bestimmten Merkmalen des Immunsystems (den HLA-Typen; humane Leukozytenantigene) ausreichend gleichen. Diese genetischen Merkmale von Interesse für die Transplantationsimmunologie liegen auf dem 6. Chromosom, und werden gebündelt vererbt. Jeder Mensch erhält einen Satz Merkmale von Vater und Mutter. Jedes Geschwisterpaar hat entsprechend eine 25%ige Chance, zwei idente Stränge von Vater und Mutter geerbt zu haben; eine 50%ige Wahrscheinlichkeit, in einem Strang übereinzustimmen, und eine 25%ige Wahrscheinlichkeit in keinem der Merkmalsstränge übereinzustimmen.
Selbst wenn Spender:in und Empfänger:in komplett HLA-identisch sind, so bestehen doch Unterschiede auf den Zelloberflächen (sogenannte Minor-Merkmale), was dazu führt, dass Spender:innen-Immunzellen Merkmale auf den Tumorzellen des:der Empfänger:in als fremd erkennen und so zur Heilung der Erkrankung beitragen können. Bei genetisch komplett identen eineiigen Zwillingen fehlt dieser Effekt.
Wenn in der Familie kein passende:r (HLA-idente:r) Stammzellspender:in verfügbar ist, so wird mittels eines medikamentösen Manövers ein:e halbpassende:r Spender:in (Geschwister, Elternteil oder Kind) eine sogenannte haploidentische Spende durchgeführt oder eine Fremdspender:innensuche eingeleitet. Für sehr viele Patient:innen kann unter den über 40 Millionen weltweit registrierten freiwilligen Personen ein:e Spender:in identifiziert werden. In seltenen Fällen kann es erforderlich sein, auf Stammzellen aus Nabelschnurblut zurückzugreifen.
Die Stammzellspende
Vor einer Stammzellspende wird jede:r potentielle:r Spender:in ausführlich medizinisch abgeklärt, um sicherzustellen, dass die Spende keine Gefährdung für den:die Spender:in darstellt. Die Spender:innen-Sicherheit steht stets an wichtigster Stelle.
Knochenmarkspende durch Punktion des Beckenknochens
Die Knochenmarkentnahme durch Punktion des hinteren Beckenkamms in Vollnarkose: Der:Die Spender:in befindet sich hierbei in Bauchlage, zwei Operateur:innen entnehmen mittels Punktionsnadel maximal 20ml/kg Knochenmarksblut (sprich bis zu 1–1,5 Liter). Wenngleich sich meist nur 2 Punktionsstellen pro Seite in der Haut finden, so wird der Knochen selbst doch mehrfach punktiert, was in den ersten Tagen und Wochen nach der Spende Schmerzen bereiten kann. Ebenso kann der Blutverlust anfänglich spürbar sein, normalisiert sich jedoch schon bald darauf wieder.
Knochenmarkspende mittels Blutspende und Apherese
Häufiger werden Blutstammzellen aus dem Knochenmark mittels Wachstumsfaktor ins Blut mobilisiert: Hierfür wird über 5 Tage ein Wachstumfaktor (G-CSF) zuhause eigenständig verabreicht (subcutan). Dadurch wird die unreife Blutbildung und Proliferation (Vermehrung) der Stammzellen enorm gesteigert, sodass die Stammzellen nach wenigen Tagen aus dem Knochenmark ins Blut übertreten. Diese Überstimulation der Blutbildung ist meist spürbar als teils pulsierende Schmerzen der großen Knochen (vor allem Becken, Wirbelsäule, Oberschenkel, aber auch Brustbein und Schädel) und grippeartige Symptome. Die frühzeitige Einnahme von Paracetamol kann die Beschwerden mildern.
Üblicherweise am 5. Tag der Stimulation kann die Stammzellsammlung mittels Apherese erfolgen. Hierfür wird das Vollblut über eine großlumige Entnahmekanüle in eine Maschine (Zellseparator) geleitet, in welcher durch Zentrifugation das Blut nach Größe und Gewicht aufgetrennt wird. Die Schicht, in der sich die Blutstammzellen befinden, wird abgeleitet, das Restblut wird dem:der Spender:in zurückgeführt, sodass der absolute Blutverlust gering ist. Eine derartige Aphereseprozedur dauert ca. 4–5 Stunden - beim Großteil der gesunden Spender:innen reicht eine einmalige Apheresesitzung, um ausreichend Stammzellen zu gewinnen, selten (z.B. Spender:in mit geringem Gewicht spendet für Empfänger:in mit deutlich höherem Körpergewicht) ist jedoch ein zweiter Sammeltag erforderlich. Bei günstigen Venenverhältnissen kann die Stammzellentnahme über 2 großlumige Zugänge an beiden Armen erfolgen, bei ungünstigen Venenverhältnissen ist die Einlage eines zentralen Venenkatheters über eine Halsvene erforderlich.
Die gewonnenen Blutstammzellen werden im Normalfall frisch verabreicht. Seit Pandemiezeiten werden die Zellen aus logistischen Gründen teilweise aber auch zunächst in flüssigem Stickstoff tiefgefroren aufbewahrt bis zur eigentlichen Transplantation.
Abstoßung
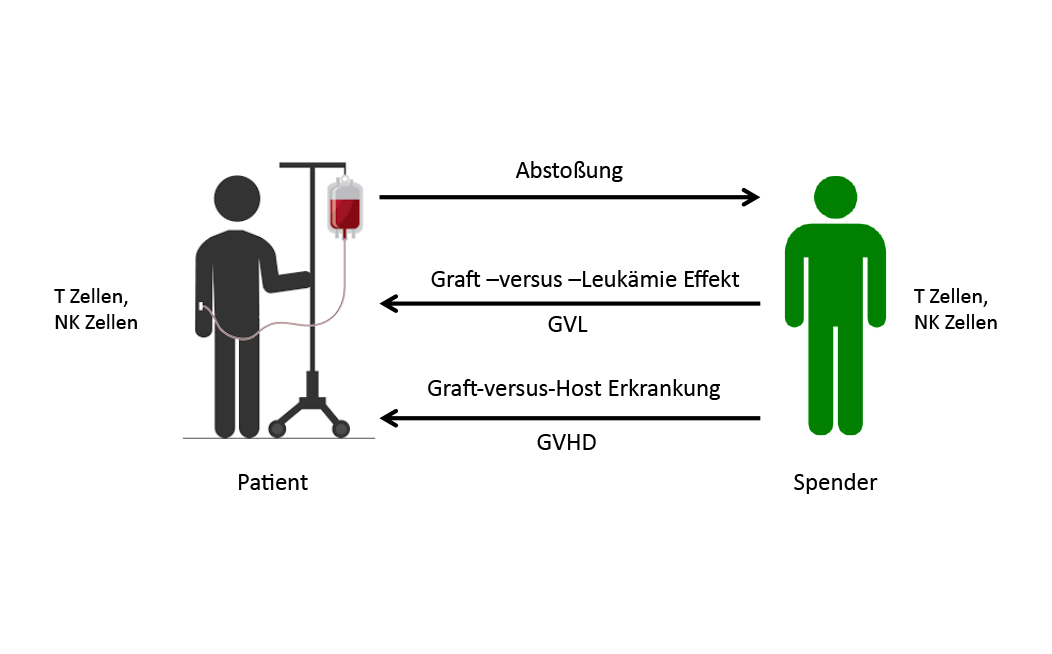
Trotz HLA-Identität bestehen vielfältige Unterschiede zwischen Spender:in und Empfänger:in, welche zu einer Graft-versus-Host-Erkrankung (GVHD) führen können (T-Zellen des:der Spender:in attackieren Organe des:der Empfänger:in).
Auf der anderen Seite attackieren Spender:in-T-Zellen residuelle Tumorzellen des:der Patient:in, man nennt dies Graft-versus-Leukämie-Effekt (GVL).
Allerdings kann das Immunsystem des:der Empfänger:in, vor allem wenn es zum Zeitpunkt der Transplantation noch aktiv ist (z.B. zu geringe Konditionierungstherapie), zu einer Abstoßung der Spender:innen-Zellen führen.